DS. Hà Phương Thảo
Khoa Dược- Bệnh viện Giao thông vận tải
Nguồn gốc kháng sinh Linezolid
Linezolid là đại diện đầu tiên của kháng sinh nhóm oxazolidinon. Năm 1987, các nhà khoa học tại E.I. du Pout de Nemours & Co. đã tìm ra loại chất kháng khuẩn mới có hoạt tính kháng khuẩn mạnh, đó là các oxazolidinon[6]. Vào những năm 1990, khi sự gia tăng của các vi khuẩn Gram dương đa kháng như tụ cầu vàng kháng methicillin (MRSA) hoặc cầu khuẩn ruột kháng vancomycin (VRE) ngày càng trở thành vấn đề lớn trên lâm sàng, thì việc tìm ra các kháng sinh có hoạt tính tốt chống lại các vi khuẩn Gram dương như kháng sinh nhóm oxazolidinon càng trở nên cần thiết[5]. Các nghiên cứu sau đó đã tìm ra hai hợp chất có hoạt tính kháng khuẩn vượt trội cùng với đặc điểm an toàn phù hợp là linezolid và eperezolid. Tuy nhiên trong nghiên cứu lâm sàng pha 1, so với eperezolid, linezolid có đặc điểm dược động học (sinh khả dụng đường uống, tỷ lệ gắn với protein huyết tương) vượt trội hơn nên chỉ cần dùng 2 lần/ngày, do đó linezolid được lựa chọn tiếp tục nghiên cứu ở pha 2[17]. Sau đó, linezolid đã được FDA Hoa Kỳ phê duyệt vào tháng 4 năm 2000[2].
Cấu trúc hóa học của linezolid
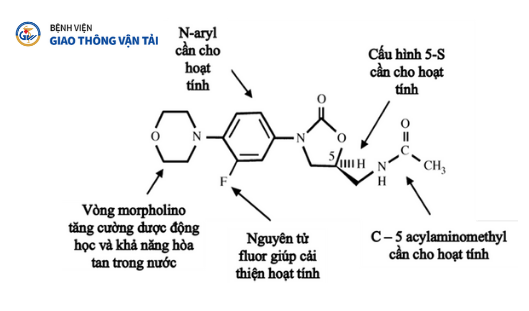
Hình 1.1. Liên quan cấu trúc – tác dụng của linezolid [7]
Linezolid là một chất tương tự morpholinyl của piperazinyl oxazolidinon, với fluor ở vị trí 3-phenyl giúp tăng cường hoạt động kháng khuẩn. Với công thức hóa học C16H20FN3O4, trọng lượng phân tử 337,35D, linezolid là (S)-N-((3-(3-fluoro-4-(4 morpholinyl) phenyl)-2-oxo-5-oxazolidinyl) methyl)-acetamide (Hình 1.1)[7].
Cơ chế tác dụng
Các oxazolidinon có cơ chế tác dụng độc đáo - ngăn chặn sự hình thành phức hợp khởi đầu trong quá trình tổng hợp protein. Không giống các kháng sinh ức chế tổng hợp protein khác như tetracyclin, chloramphenicol, aminoglycosid, macrolid và streptrogramin - cho phép bắt đầu dịch mã mRNA nhưng sau đó ức chế sự kéo dài chuỗi peptid. Sự khác biệt về cơ chế hoạt động này giúp linezolid không bị kháng chéo với các loại kháng sinh hiện có[2].
Linezolid ức chế tổng hợp protein của vi khuẩn bằng cách ngăn chặn sự hình thành phức hợp khởi đầu của N-formylmethionyl-tRNA-mRNA-70S. Linezolid liên kết với trung tâm 23S peptidyl transferase của tiểu đơn vị 50S của ribosom, ngăn cản sự hình thành phức hợp khởi đầu 70S - phức hợp khởi động chức năng tổng hợp protein, do đó ngăn cản quá trình dịch mã mRNA [2](Hình 1.2). Thêm vào đó, linezolid đã được báo cáo rằng với nồng độ 1/2, 1/4, 1/8 MIC linezolid với S. aureus, thuốc ức chế sản xuất α-haemolysin, δ-haemolysin và coagulase - các độc tố gây ly giải tế bào, tan huyết. Đối với S. pyogenes, linezolid ức chế tổng hợp streptolysin O - độc tính với nhiều loại tế bào, deoxyribonuclease với nồng độ 1/2, 1/4, 1/8 MIC linezolid[8]. Điều này có thể góp phần vào tác dụng dược lý của nó trong điều trị các bệnh nhiễm trùng Gram dương nghiêm trọng và hội chứng sốc nhiễm độc[8].
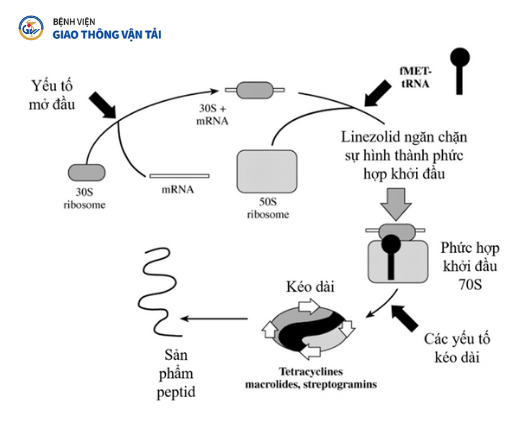
Hình 1.2. Cơ chế tác dụng của linezolid [9]
Phổ tác dụng
Linezolid có hoạt tính in vitro với nhiều loại vi khuẩn: hầu hết các vi khuẩn Gram dương, một số vi khuẩn Gram âm, vi khuẩn kỵ khí và vi khuẩn không điển hình[13].
Linezolid đã được phê duyệt điều trị một số nhiễm khuẩn do S.aureus (MSSA và MRSA), S.pneumoniae, S.pyogenes, S.agalactiae và E.faecium kháng vancomycin. Các vi khuẩn nhạy cảm và đề kháng được trình bày ở Bảng 1.1[1].
Bảng 1.1. Phổ tác dụng của linezolid
.png)
Ủy ban châu Âu về thử nghiệm độ nhạy cảm với kháng sinh (EUCAST) và Viện tiêu chuẩn lâm sàng và xét nghiệm Hoa Kỳ (CLSI) ghi nhận các điểm gãy nhạy cảm theo nồng độ ức chế tối thiểu (MIC) của linezolid được trình bày trong Bảng 1.2[16], [15].
Bảng 1.2. Điểm gãy nhạy cảm của linezolid với một số vi khuẩn theo EUCAST và CLSI
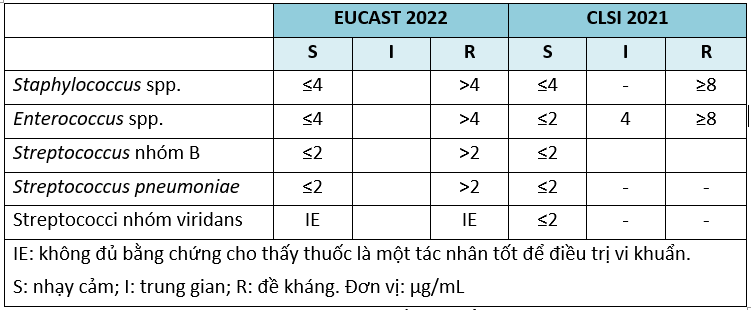
Linezolid có hoạt tính in vitro trên một số vi khuẩn Gram âm, kỵ khí. Tuy nhiên, không có nghiên cứu in vivo có kiểm soát nào về hiệu quả của linezolid trong điều trị các tác nhân này[14].
Linezolid thể hiện hoạt tính in vitro chống lại cả vi khuẩn lao Mycobacterium tuberculosis, kể cả chủng đã kháng với các tác nhân chống lao tiêu chuẩn mà không có đề kháng chéo[2]. Tuy nhiên, với bệnh nhân mắc lao đa kháng, linezolid được khuyến cáo nên sử dụng trong phác đồ dài hạn[18]. Việc dùng linezolid trên sáu tháng có thể tăng hiệu quả điều trị nhưng có thể bị hạn chế bởi các biến cố bất lợi[19]. Do đó, việc sử dụng linezolid trong điều trị lao đa kháng hạn chế và cần được theo dõi nồng độ thuốc trong điều trị để giảm nguy cơ gặp các biến cố bất lợi[13].
Tình hình đề kháng linezolid
Trong số các tụ cầu, kháng linezolid dường như xảy ra thường xuyên nhất ở các chủng tụ cầu âm tính với coagulase, chủ yếu là Staphylococcus epidermidis. Chương trình LEADER báo cáo tỷ lệ đề kháng linezolid từ 0,03 đến 1,83% khi thử nghiệm với hơn 42.419 chủng tụ cầu và cầu khuẩn phân lập lâm sàng trong 9 năm giám sát liên tiếp (2004 - 2012) tại Hoa Kỳ. Chương trình ZAAPS đã ghi nhận tỷ lệ không nhạy cảm với linezolid thậm chí còn thấp hơn (≤ 1,2%) trong số tụ cầu và cầu khuẩn từ các bệnh viện ngoài Hoa Kỳ. Cụ thể hơn, tỷ lệ không nhạy cảm với S. aureus được ghi nhận trong chương trình LEADER tăng từ năm 2004 đến năm 2009, duy trì ổn định trong giai đoạn sau (2010-2012). Tỷ lệ đề kháng với linezolid đối với tụ cầu âm tính với coagulase cho thấy xu hướng đề kháng tổng thể tăng nhẹ trong các chương trình ZAAPS, trong khi tỷ lệ tăng đã được quan sát thấy trong chương trình LEADER từ năm 2004 đến năm 2008 và giảm trong những năm tiếp theo. Tỷ lệ đề kháng với Enterococci tăng lên đạt mức cao nhất vào năm 2006 đối với cả hai chương trình ZAAPS và LEADER, dao động tương ứng trong khoảng 0,4-0,7% và 0,3-1,0% trong giai đoạn tiếp theo[11]. Tuy nhiên, sự đề kháng của S. aureus với linezolid, dù không thường xuyên, cũng đã được ghi nhận [12].
Enterococcus faecium kháng vancomycin kháng với linezolid cũng đã được mô tả[4]. Sự đề kháng ở Enterococci cũng không thường xuyên, xảy ra ở <1% số chủng phân lập trong các nghiên cứu giám sát lớn. Một đánh giá có hệ thống đã được thực hiện đối với các tài liệu hiện có về cầu khuẩn ruột kháng linezolid (LRE) để xác định đặc điểm của các bệnh nhiễm trùng này liên quan đến các đặc điểm dịch tễ, vi sinh và lâm sàng. Các kết quả đã xác nhận hiệu lực của linezolid điều trị nhiễm trùng do liên cầu, với tỷ lệ nhạy cảm bền vững là 99,8% trong chương trình ZAAPS và 99,2% trong các chương trình LEADER. Bệnh nhân nhiễm cầu khuẩn ruột kháng linezolid chủ yếu tiếp xúc với linezolid trước khi xuất hiện cầu khuẩn ruột kháng linezolid, với thời gian điều trị trung bình là 29,8±48,8 ngày đối với Enterococcus faecalis và 23,1±21,4 ngày đối với Enterococcus faecium. Tuy nhiên, cầu khuẩn ruột kháng linezolid cũng có thể phát triển ở những bệnh nhân không tiếp xúc với linezolid trước đó. Kháng linezolid được cho là do đột biến 23S rRNA (G2576T) (51,2% E. faecalis và 80,5% E. faecium) cũng như sự hiện diện của gen cfr (tương ứng là 4,7% và 4,8%), có thể di truyền theo chiều ngang giữa các các chủng. Ngoài gen cfr ở 32 trường hợp cầu khuẩn ruột dương tính với optrA đã được xác định, cần phải nghiên cứu thêm để xác định sự phổ biến của các gen kháng thuốc mới[3]. Đề kháng với linezolid thường xảy ra thông qua nhiều đột biến của gen 23S rRNA[10].
Tài liệu tham khảo
1. Cục quản lý dược "Tờ hướng dẫn sử dụng thuốc Zyvox", https://drugbank.vn/, pp.
2. Zahedi Bialvaei A. Rahbar M., et al. (2017), "Linezolid: a promising option in the treatment of Gram-positives", J Antimicrob Chemother, 72(2), pp. 354-364.
3. Bi R. Qin T., et al. (2012), "The emerging problem of linezolid-resistant enterococci", J Glob Antimicrob Resist, 13, pp. 11-19.
4. Dobbs T. E. Patel M., et al. (2006), "Nosocomial spread of Enterococcus faecium resistant to vancomycin and linezolid in a tertiary care medical center", J Clin Microbiol, 44(9), pp. 3368-3370.
5. Douros Antonios Grabowski Katja, et al. (2015), "Drug–drug interactions and safety of linezolid, tedizolid, and other oxazolidinones", Expert opinion on drug metabolism & toxicology, 11(12), pp. 1849-1859.
6. Ford C. W. Hamel J. C., et al. (1997), "Oxazolidinones: new antibacterial agents", Trends Microbiol, 5(5), pp. 196-200.
7. Fung Horatio B Kirschenbaum Harold L, et al. (2001), "Linezolid: an oxazolidinone antimicrobial agent", Clinical therapeutics, 23(3), pp. 356-391.
8. Gemmell C. G. Ford C. W. (2002), "Virulence factor expression by Gram-positive cocci exposed to subinhibitory concentrations of linezolid", J Antimicrob Chemother, 50(5), pp. 665-672.
9. M. Livermore D. (2003), "Linezolid in vitro: mechanism and antibacterial spectrum", J Antimicrob Chemother, 51(2), pp. 9-16.
10. Meka V. G. Gold H. S. (2004), "Antimicrobial resistance to linezolid", Clin Infect Dis, 39(7), pp. 1010-1015.
11. Mendes R. E. Deshpande L. M., et al. (2014), "Linezolid update: stable in vitro activity following more than a decade of clinical use and summary of associated resistance mechanisms", Drug Resist Updates, 17(1-2), pp. 1-12.
12. Morales G. Picazo J. J., et al. (2010), "Resistance to linezolid is mediated by the cfr gene in the first report of an outbreak of linezolid-resistant Staphylococcus aureus", Clin Infect Dis, 50(6), pp. 821-825.
13. Rao G. G. Konicki R., et al. (2020), "Therapeutic Drug Monitoring Can Improve Linezolid Dosing Regimens in Current Clinical Practice: A Review of Linezolid Pharmacokinetics and Pharmacodynamics", Ther Drug Monit, 42(1), pp. 83-92.
14. Stevens D. L. Dotter B., et al. (2004), "A review of linezolid: the first oxazolidinone antibiotic", Expert Rev Anti Infect Ther, 2(1), pp.
15. Testing European Committee on Antimicrobial Susceptibility (2022), "Breakpoint tables for interpretation of MICs and zone diameters. Version 12.0, valid from 2022-01-01", https://www.eucast.org/fileadmin/src/media/PDFs/EUCAST_files/Breakpoint_tables/v_12.0_Breakpoint_Tables.pdf., pp.
16. Weinstein Melvin P. II James S. Lewis, et al. (2021), M100 – Performance Standards for Antimicrobial Susceptibility Testing, 31st Edition, pp.
17. Zurenko Gary E Ford Charles W, et al. (1997), "Oxazolidinone antibacterial agents: development of the clinical candidates eperezolid and linezolid", Expert opinion on investigational drugs, 6(2), pp. 151-158.
18. Bộ Y tế (2021), "Quyết định 2760/QĐ-BYT ban hành ngày 03/06/2021 về việc ban hành “Cập nhật hướng dẫn điều trị lao kháng thuốc”", pp.
19. Bộ Y tế (2020), "Quyết định 1314/QĐ-BYT ban hành ngày 24/03/2020 về việc ban hành “Hướng dẫn chẩn đoán, điều trị và dự phòng bệnh lao”", pp.




