DS. Nguyễn Thị Linh Trang
Khoa Dược - Bệnh viện Giao thông vận tải
ĐỘC TÍNH TRÊN THẬN:
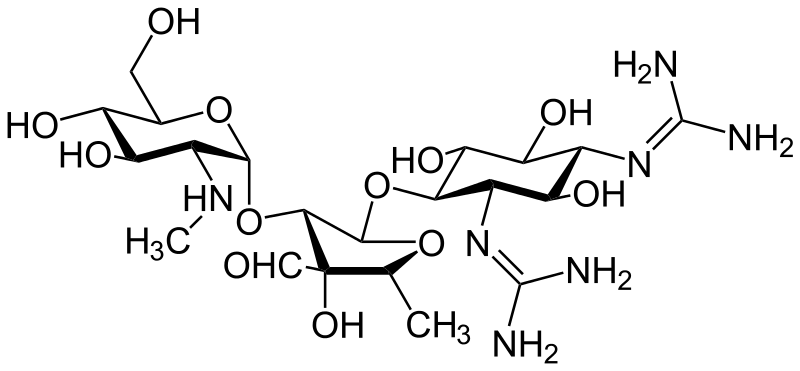
Cấu trúc Polyamin của phân tử Aminoglycoside
Cơ chế bệnh sinh:
Tổn thương thận cấp (AKI) do hoại tử ống thận là một biến chứng thường gặp khi điều trị với kháng sinh aminoglycoside. Nồng độ creatinin huyết thanh được ghi nhận tăng từ 0.5 đến 1 mg/dL (44 đến 88 micromol/l) hoặc hơn 50% so với mức creatinin huyết thanh nền ở 10% đến 20% bệnh nhân trưởng thành, 20% đến 33% bệnh nhân nhi, đặc biệt ở những bệnh nhân phải chăm sóc đặc biệt.
Aminoglycoside được lọc tự do và thải trừ hoàn toàn qua cầu thận, chỉ với 5% đến 10% liều tiêm tĩnh mạch được tái hấp thu và lưu giữ tại tế bào ống lượn gần - đây cũng chính là nguyên nhân gây độc cho thận. Nhiều nhóm amin trên phân tử aminoglycoside tạo ra liên kết tĩnh điện với anion phospholipid trên màng tế bào ống lượn gần. Sự gắn kết giữa phân tử aminoglycoside với phospholipid màng dẫn đến sự ức chế hoạt tính phospholipase trong lysosom, và có thể là nguyên nhân gây ra tình trạng phospholipid niệu và phospholipid vỏ thận (còn được hiểu là quá trình tích luỹ của các chất có cấu trúc đa lớp giống myelin ở vỏ thận, chứa phospholipid và protein). Một điều thú vị là, ái lực tương đối giữa phospholipid màng với aminoglycoside tương quan với độc tính trên thận, cụ thể:
- Neomycin có ái lực cao nhất với phospholipid trên tế bào ống thận, nên có độc tính cao nhất.
- Tobramycin và Gentamicin có ái lực thấp hơn, do đó độc tính trên thận thấp hơn.
- Amikacin có ái lực liên kết yếu hơn, do đó độc tính thấp hơn Tobramycin và Gentamicin.
Ngoài ra, aminoglycoside còn được vận chuyển đến protein xuyên màng Megalin và được nhập bào. Megalin là một thụ thể nhặt rác bề mặt và có ái lực cao với protein, cũng như các vùng chứa axit amin mang điện tích dương. Nó được biểu hiện ở nhiều mô trong cơ thể, trong đó có các tế bào ở các ống lượn gần. Sau khi xảy ra quá trình nhập bào, các endosome chứa aminoglycoside được vận chuyển và hòa nhập với các lysosom, sau đó chúng được vận chuyển đến bộ máy Golgi. Từ bộ máy Golgi, các phân tử aminoglycoside lại được vận chuyển đến lưới nội chất, rồi chúng tích tụ thành các cấu trúc trong bào tương, ức chế hoạt động của ty thể. Chúng kích hoạt quá trình chết tế bào theo chương trình, làm gián đoạn chuỗi hô hấp, làm suy yếu quá trình sản xuất ATP, tạo ra stress oxy hóa bằng cách tăng superoxide anion và gốc hydroxyl, góp phần làm chết tế bào.
Các chiến lược phòng ngừa:
Khi sử dụng aminoglycoside trên lâm sàng, có thể cân nhắc các biện pháp dưới đây để giảm thiểu độc tính của thuốc trên thận:
- Lựa chọn aminoglycoside ít độc nhất nếu có thể. Gentamicin được xem là chất gây độc cho thận nhất. Các thuốc còn lại có độc tính giảm dần theo thứ tự: tobramycin, amikacin, neltimicin và streptomycin.
- Giải quyết tình trạng hạ kali máu và magie máu trước khi dùng aminoglycoside.
- Aminoglycoside là kháng sinh có hiệu quả phụ thuộc nồng độ,và có tác dụng hậu kháng sinh kéo dài. Nhiều nghiên cứu đã chứng minh hiệu quả của việc dùng liều duy nhất trong ngày tương đương với cách dùng thuốc truyền thống là 2-3 lần/ngày, nhưng có thể mang lại những ưu điểm vượt trội như:
- Ít gây độc tính trên thận hơn.
- Dễ quản lý và theo dõi nồng độ thuốc trong huyết thanh, từ đó giảm chi phí liên quan đến quản lý và giám sát sử dụng thuốc.
- Giảm nguy cơ xuất hiện đề kháng thuốc.
- Một số liều dùng gợi ý của các kháng sinh ở người lớn, có chức năng thận bình thường, với chế độ liều 1 lần/ngày.
- Gentamicin, Tobramycin: 3-8 mg/kg cân nặng/ngày.
- Netilmycin: 4-8 mg/kg cân nặng/ngày
- Amikacin: 15-30 mg/kg cân nặng/ngày
- Bệnh nhân suy thận có nhiều khả năng bị nhiễm độc do aminoglycoside hơn khi dùng liều cao. Do đó, với những bệnh nhân suy thận có độ thanh thải creatinin dưới 30 ml/phút, hoặc cần điều trị thay thế thận, chế độ dùng liều truyền thống (2-3 lần/ngày) nên được cân nhắc.
- Theo dõi độc tính: Nên theo dõi nồng độ creatinin huyết thanh ngay từ đầu và lặp lại sau một đến ba ngày, tùy thuộc vào từng trường hợp.
- Tránh dùng aminoglycoside ở những bệnh nhân có suy giảm thể tích tuần hoàn, hiệu chỉnh liều phù hợp với chức năng thận, giới hạn thời gian điều trị từ 7 đến 10 ngày, và giảm thiểu việc dùng cùng các thuốc khác gây độc cho thận.
- Theo dõi nồng độ thuốc trong huyết thanh:
- Việc xác định nồng độ đỉnh trong huyết thanh sau khi tiêm mũi đầu tiên được khuyến cáo với tất cả bệnh nhân nặng, đặc biệt ở bệnh nhân có thay đổi về dược động học như bệnh nhân sốc nhiễm khuẩn, bỏng, bệnh nhân béo phì, chấn thương, xơ nang,….
Việc xác định nồng độ đỉnh trong huyết thanh sau khi tiêm mũi đầu tiên được khuyến cáo với tất cả bệnh nhân nặng, đặc biệt ở bệnh nhân có thay đổi về dược động học như bệnh nhân sốc nhiễm khuẩn, bỏng, bệnh nhân béo phì, chấn thương, xơ nang,….
Việc xác định nồng độ đỉnh nên được tiến hành trong 30 phút sau khi kết thúc truyền thuốc.
Nếu kết quả thấp hơn so với nồng độ đỉnh cần đạt được thì cần phải tăng liều ở lần tiêm sau.
Xác định nồng độ đáy của thuốc chỉ cần thiết khi độ dài đợt điều trị lớn hơn 5 ngày (tiến hành đánh giá sau 48 giờ điều trị) hoặc trong trường hợp có suy giảm chức năng thận và cần phải được tiến hành 2 lần/tuần cùng với việc đánh giá chức năng thận.
Nếu nồng độ đáy của thuốc đo được cao hơn nồng độ trong Bảng 1 thì cần phải tăng khoảng cách giữa các lần đưa thuốc vì nồng độ đáy là yếu tố liên quan đến độc tính trên thận của thuốc.
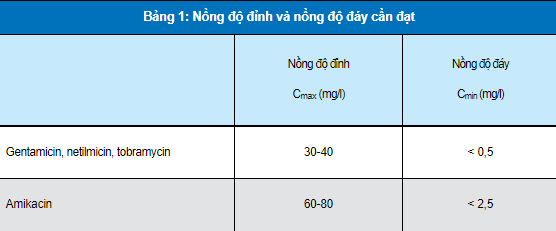
Bảng 1: Mục tiêu nồng độ đỉnh và nồng độ đáy cần đạt của kháng sinh aminoglycoside
Độc tính trên tai
Aminoglycoside có liên quan đến độc tính ốc tai và tiền đình ở một tỷ lệ đáng kể bệnh nhân dùng thuốc trong thời gian dài, dẫn đến mất thính lực và mất cân bằng.
Gentamicin và tobramycin chủ yếu gây độc cho tiền đình; trong khi đó neomycin, kanamycin và amikacin gây độc trên tai nhiều hơn.
Cơ chế bệnh sinh:
Một giả thuyết có liên quan đến các thụ thể N-methyl-D-aspartate (NMDA), hiện diện ở synape giữa tế bào lông ở ốc tai và tế bào thần kinh hướng tâm. Aminoglycoside có thể bắt chước khả năng gây kích thích và làm tổn thương của các polyamine tại các thụ thể này. Nghiên cứu trên động vật cho thấy, việc sử dụng các chất đối kháng NMDA có thể làm suy giảm rõ rệt tình trạng mất thính lực phù hợp với giả thiết này.
Ngoài những thay đổi về chức năng, aminoglycoside còn làm thay đổi về cấu trúc, như làm thay đổi tính bảo tồn và thoái hóa của các tế bào hạch xoắn ốc của ốc tai.
Aminoglycoside tạo ra những phản ứng oxy hóa phá hủy tế bào tai trong. Các thử nghiệm invitro và thử nghiệm trên động vật đã tìm thấy những loại phản ứng oxy hóa gây ra bởi aminoglycoside ủng hộ cho giải thiết này.
Ngoài ra, có giả thiết cho rằng, đột biến điểm tại Ribosome ARN 12S có tính di truyền, có thể làm tăng tính nhạy cảm với nhiễm độc tai khi sử dụng aminoglycoside.
Các biện pháp phòng ngừa nhiễm độc tai:
Các chiến lược được sử dụng để ngăn ngừa nhiễm độc tai do aminoglycoside tương tự như các chiến lược trong phòng ngừa nhiễm độc thận, bao gồm:
1. Cân nhắc chế độ dùng thuốc 1 lần/ngày và theo dõi cẩn thận nồng độ thuốc trong máu.
2. Theo dõi độc tính trên tai dựa trên những đánh giá chủ quan của người bệnh về sự rối loạn chức năng thính giác và tiền đình. Việc sử dụng các xét nghiệm để đánh giá như đo thính lực hay ghi điện nhãn đồ chỉ sử dụng với những bệnh nhân có triệu chứng rối loạn thính giác trước đó, hoặc cho bệnh nhân cần điều trị kéo dài.
3. Khai thác tiền sử gia đình bệnh nhân để xác định nguy cơ gặp phải độc tính trên tai do aminoglycoside gây ra. Với những bệnh nhân có nguy cơ cao, có thể sử dụng kháng sinh khác có phổ trên vi khuẩn Gram (-) để điều trị thay thế.
4. Dựa trên giả thuyết về phản ứng oxy hóa do aminoglycoside gây ra, N-acetylcysteine (NAC)- một chất chống oxy hóa chứa thiol được nghiên cứu sử dụng ở những bệnh nhân chạy thận nhân tạo sử dụng gentamicin.
Tổng quan về nghiên cứu sử dụng NAC trên bệnh nhân dùng gentamicin
| Đối tượng nghiên cứu: 53 bệnh nhân chạy thận nhân tạo bị nhiễm khuẩn huyết do ống thông. |
| Phương pháp nghiên cứu: Những bệnh nhân này được chia làm 2 nhóm ngẫu nhiên: + Nhóm 1: Chỉ được sử dụng Gentamicin + Nhóm 2: Sử dụng Gentamicin kết hợp với NAC (600mg/2 lần/ngày, cho đến một tuần sau khi kết thúc liệu pháp kháng sinh) Thính lực được đo vào thời điểm ban đầu khi chưa dùng thuốc, sau một tuần và sau 6 tuần khi kết thúc điều trị kháng sinh. |
| Kết quả: + Liệu pháp kết hợp với NAC làm giảm đáng kể tỷ lệ nhiễm độc thính giác (25% so với 60%). + Nhóm dùng NAC không gặp bất cứ tác dụng bất lợi nào. |
| Bình luận: Cần có thêm những nghiên cứu với cỡ mẫu lớn hơn để chứng minh hiệu quả của NAC trong việc giảm nguy cơ gây độc tính trên tai của aminoglycoside. Tuy nhiên, với sự an toàn đã được chứng minh của NAC, cùng với đó là nguy cơ gây độc tính trên tai không hồi phục của aminoglycoside, NAC là một giải pháp tiềm năng có thể cân nhắc sử dụng trên lâm sàng, đặc biệt trên đối tượng bệnh nhân chạy thận nhân tạo phải sử dụng aminoglycoside. |
TÀI LIỆU THAM KHẢO
- Uptodate (05/11/2021); Bruce A Molitoris,MD. “Pathogenesis and prevention of aminoglycoside nephrotoxicity and ototoxicity.”
- Uptodate (16/12/2022); Richard H Drew, PharmD, MS, FCCP, FIDP. “Dosing and administration of parenteral aminoglycosides.”
- Jose M. Lopez-Novoa (01/11/2011), “New insights into the mechanism of aminoglycoside nephrotoxicity: an integrative point of view.”
- Cảnh giác Dược (2016), Bản tin cảnh giác Dược quý II, năm 2016






.png)
_thumb_150.png)